�P(gu��n)���҂�
�īI(xi��n)����حNat Rev Cancer�[�����x��չ��δ��

�[�����x�ǽ�����[������W(xu��)�о��ğ��c(di��n)֮һ���[����(x��)�������{(di��o)�صĴ��x��׃���������ǽͽ⣨WarburgЧ��(y��ng)���������ǔzȡ�����ӡ��Ȱ��������x�������S�����÷���Ҫ�������|(zh��)���ܵȣ��@Щ��׃�M�����[����(x��)��������ֳ�r��ʢ�����������|(zh��)��������(x��)���m��(y��ng)ȱ�����[���h(hu��n)�����M(j��n)�����[������ֳ�����u���w�Ƶ��������ṩ���������|(zh��)֧�֡�
�[���l(f��)���Ͱl(f��)չ��Ҫ�[����(x��)���Ĵ��x�ؾ��̡�����������W(xu��)Navdeep Chandel�F(tu��n)�(du��)ȫ��śr���[�����x�I(l��ng)��������о��M(j��n)չ���������˱��I(l��ng)������δ��Q���P(gu��n)�I���}���C�����¡�Cancer metabolism: looking forward����2021��7�°l(f��)����Nature reviews cancer�ϡ�
�vʷ����
1921����ƌW(xu��)��Otto Warburg�^�쵽һ�N��ֵĬF(xi��n)���[����(x��)�����ǽͽ⮐�����S����ʹ���������ėl���£��[����(x��)��Ҳ�A���ڌ������ǡ��l(f��)�͡������ᡣ������Ҳ��?y��n)�l(f��)�F(xi��n)��(x��)�����������D(zhu��n)��ø���@����1931����Z����Warburg����y�[����(x��)���ľ����w���ڰl(f��)��ȱ�ݣ��Ķ���(d��o)���������������ܓp���ʶ���ه���ǽͽ���x�����ǣ��S����о������������(sh��)�[����(x��)���о����w���ܲ�δ�ܓp�������[����(x��)���������ǽͽ����������ጡ�20���o(j��)90������˂��J(r��n)�R�����c�ǽͽ������Ó��øA��LDHA���ǰ�����MYC���D(zhu��n)䛰��c(di��n)���@��WarburgЧ��(y��ng)�ṩ�˷��ӻ��A(ch��)�����⣬ͬ��߀�l(f��)�F(xi��n)��AKT��mTOR��HIF��ʧ�{(di��o)���@ЩҲ���[����������L������ġ��@Щ;���քeͨ�^�������D(zhu��n)�\(y��n)�����ǽͽ�ø���D(zhu��n)����{(di��o)�����ữ�������ǽͽ⡣
�ڱ����o(j��)�����ֵ��о�������������WarburgЧ��(y��ng)�ęC(j��)���о�����ʲô���������[�������L��һ�N�����ͨ�^�����ǽͽ⣬�ǽͽ�����g�a(ch��n)������M(j��n)��ϳɴ��xͨ·ȥ֧�ֺ����ᡢ֬�������ĺϳɏĶ�ʹ��(x��)����ֳ����һ�N�µĽ����TCAѭ�h(hu��n)��Փ��һ���P(gu��n)�I���C��(j��)��ͨ�^�[����(x��)���е���ӂ��f朣�ETC�����́��l(f��)�F(xi��n)�ģ�����ETC���P(gu��n)��TCAѭ�h(hu��n)������ã���ͨ�^�������ữ�Ɖ���ETC���P(gu��n)��ATP���ɣ��[����Ȼ�ڻ��w��(n��i)���L���@���������ǽͽ��ATP����֧��ԭ�l(f��)���[�����L�����⣬��ͪ���Ȼ�ø��PC��ʹ��ͪ������TCAѭ�h(hu��n)���x�a(ch��n)��������ᣬҲ���C����ԭ�l(f��)�Ժ��D(zhu��n)�����[�����L����������|(zh��)����������a(ch��n)�����춬���ἰ���������춬���������������[�����L�����⣬�������x�a(ch��n)���Ļ�������ROS�����Ԍ�(d��o)���[���l(f��)��������Ҫ��(y��n)���{(di��o)��(ji��)����������(x��)���������@ƪ���²����Ǟ����ṩ�P(gu��n)���[�����x��Ҫ�I(l��ng)��������о���Ԕ��(x��)��Ϣ�������ṩ��һ��ҕ�ǣ����L�˹������}���P(gu��n)�I���}��
�ϳɴ��x�c�[�����L
�a(ch��n)���ɂ��Ӽ�(x��)����Ҫ��(x��)����ֳ�^���еĴ���ӣ�����������֬�|(zh��)�����[����(x��)���ɏ�ѪҺѭ�h(hu��n)�Ы@��������(x��)���ϳɵĴ���ӡ��ɂ��P(gu��n)�I���}�ǣ�1���[�����L�^�̵����ٴ��������Щ��2���S���[�����LҪ�{(di��o)����Щ����(n��i);�����@Щ�^�̿���ȡ�Q�ڏ��[���h(hu��n)����TME���С����ض��l���£�֬�|(zh��)�����h(hu��n)���Ы@�ã�����������r�£�����(x��)��������Ҫ���^�ϳ�֬�|(zh��)���D1����
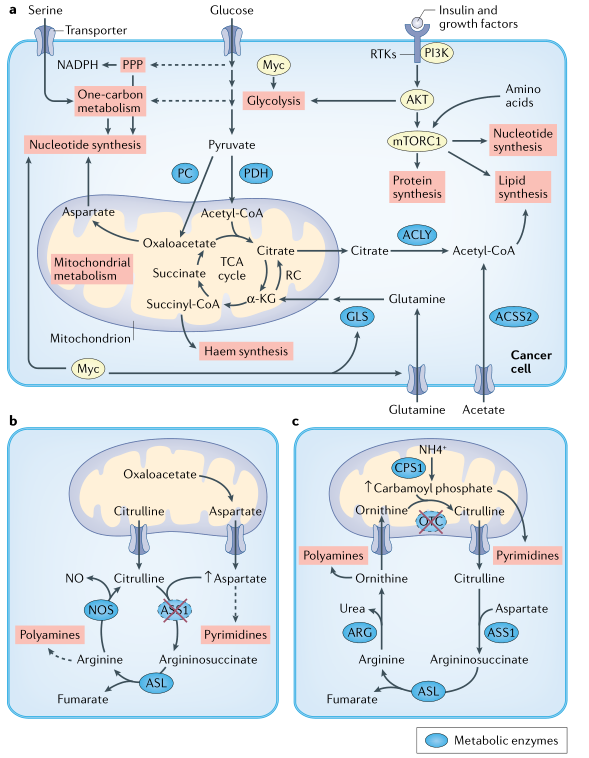
�D1֧���[���a(ch��n)���ĵĴ��x�����̖ͨ·
��̖ͨ·
�[����(x��)������x����̖ͨ·���D(zhu��n)䛾W(w��ng)�j(lu��)������PI3K-AKT-mTORC1��MYC��ͨ�^���Ӵ��xͨ�����S�ּ�(x��)����ֳ��mTORC1ͨ·�ѳɞ�I�B(y��ng)���o�����Ĺ�(ji��)�c(di��n)��ͨ�^�ӏ�(qi��ng)��(x��)���еĵ����|(zh��)�ϳɡ�֬�|(zh��)�ϳɺͺ�����ϳɵ�;����M�㼚(x��)����ֳ�����|(zh��)���A(ch��)��
������̖���ӵĴ��x��
��һЩ�[�������ڰl(f��)��������Ó��ø��SDH�����Ӻ�����ˮ��ø��FH������������Ó��ø1��2��IDH1/IDH2������ͻ׃������(y��ng)�����δ��x�������ᡢ�Ӻ������2-�u������ᣨ2HG����ˮƽ������ӣ��Ķ���(d��o)�²�ͬ�[���İl(f��)�����@Щ���x���������Q�顰�[�����x����D2�������磬SDHͻ׃��Ҋ���z���Ը���(j��ng)��(ji��)�������t��(x��)������θ�c���g�|(zh��)������FHͻ׃�Ɍ�(d��o)���z����ƽ�����������I��(x��)������IDH1/IDH2ͻ׃�Ɍ�(d��o)��đ�ܰ���ܛ���������z�|(zh��)���ͼ�����ϵ��Ѫ����Ҫע����ǣ�SDH��/��FHͻ׃���[����(x��)������Ȼ�܉�����TCAѭ�h(hu��n)���x����[����(x��)�����L���衣�������oøA����Ѫ�t�غϳɣ������������ں�����ϳɡ���ˣ�����M(j��n)�д��x�ؾ������m��(y��ng)�@Щͻ׃�����_���ϳ��[����(x��)����ֳ����Ĵ���ӣ�Ѫ�t�غͺ����ᣩ��
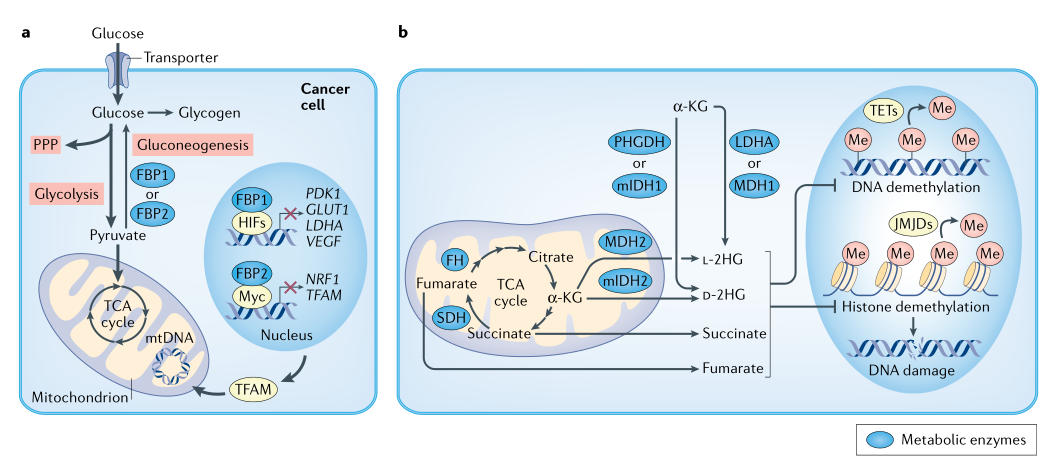
�D2���Y���x����̖�ͷǵ��͙C(j��)��
�������c�[���M(j��n)չ
�[����(x��)���a(ch��n)������Ҫ��������ROS���dz������O2-�����^�����䣨H2O2�����u�����ɻ���-OH����֬�|(zh��)�^�����䣨LOOH����H2O2��Ҫ��һ�N��̖���ӣ�����ͨ�^����߀ԭ��̖���M(j��n)����(x��)����ֳ���������u��Ҳ��ͨ�^�^������ø�ֽ��ˮ����������ʽ�Ļ���������LOOH��-OH��O2-�Ɍ�(d��o)�µ����|(zh��)��֬�|(zh��)�������w�ͺ�DNA�������Ķ��a(ch��n)�����������F�������D3�����ڷ�(w��n)����B(t��i)�£��κ����ROS��ˮƽȡ�Q��ROS�a(ch��n)�������cROS������ʡ��[����(x��)����ROS�������ʱ�������(x��)���ߵö࣬�����ٰ��о���������ROSˮƽ���[����(x��)���l(f��)���ı�Ҫ�l�������S��ROSˮƽ�t�����M(j��n)�[�����D(zhu��n)�ơ��@Щ�Y(ji��)Փ����ì�ܡ�
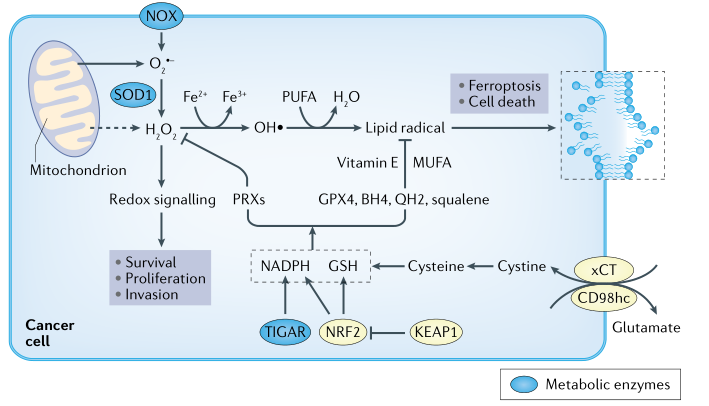
�D3�[����(x��)���е�ROS
�I�B(y��ng)����
���[���l(f��)չ�^���У���(sh��)�w�[����(n��i)�I�B(y��ng)���|(zh��)�Ŀɼ��Խ�(j��ng)���ܵ��������}��ϵ�y(t��ng)�ͽM���Y(ji��)��(g��u)��Ӱ푡��c����Ѫ�ܲ�ͬ���[���}�ܵIJ�Ҏ(gu��)�t��֧������(d��o)��ݔ�͵ĠI�B(y��ng)����R������(d��o)��TME��(n��i)�ĠI�B(y��ng)��ԡ������Ǯ�(d��ng)�I�B(y��ng)ȱ�������L���Ӳ���r����(x��)��������ֳ���P(gu��n)�I;��֮һ���D4����
TME���x
���ˠI�B(y��ng)����(y��ng)�����ԗl���ĸ�׃�⣬�w��(n��i)TME��һ�����c(di��n)�����ɲ�ͬ��͵ļ�(x��)���M�ɣ��������{(di��o)���[���M(j��n)չ��һ�����ε�ģ���ǣ���(n��i)Ƥ��(x��)���ͻ��|(zh��)��(x��)��֧���[�����L������(x��)������T��(x��)����CTLs���t�����[���M(j��n)չ����Ҫ̼���xͨ·���̼���x���ǽͽ��TCAѭ�h(hu��n)���H�ǰ���(x��)����ֳ�ı�Ҫ�l�������Ҍ���(n��i)Ƥ��(x��)�������|(zh��)��(x��)����CTLs���{(di��o)��(ji��)��T��(x��)������ϵ��(x��)���Ĺ���Ҳ���P(gu��n)��Ҫ����ˣ��[����(x��)������cTME�е��������N��(x��)�����Z�I�B(y��ng)�����磬�������D(zhu��n)�\(y��n)�w��SLC43A2��ˮƽ�����ӣ��[����(x��)��������������������ӣ��Ķ�������CTL�еĵ�����ѭ�h(hu��n)����(d��o)�½M���ױ�������Ķ���(d��o)��CTL�����ܓp��ͨ���J(r��n)�����������Ǖ������w��(n��i)�[�������L��Ȼ�����ڵ���0.5%������ˮƽ�¾����w�����������f�������ڵ���0.5 mM�������ǝ�����[����(x��)�����f������ֳ��TME�еĵ����͵�������ˮƽ���ܲ������ƴ��x����������Ӱ푻�����_(d��)��׃��������HIF�ļ�����Ķ���׃���x�m��(y��ng)���������̖ͨ·��Ȼ����ijЩ�������������TME��(n��i)�Ĵ��x�����������ᡢɫ���ᡢ�����ᡢ�z����ʰ��ᣬ�@Щ������H���[����(x��)����ֳ������ģ�Ҳ��CTL����������ġ�
���ˠI�B(y��ng)�����⣬TME�в�ͬ��ͼ�(x��)��֮�gҲ���ڴ��x��?d��ng)_��ʹ���[����(x��)�������ڲ����l�������L�����磬�������[���У����|(zh��)���P(gu��n)�����Ǡ(x��)�����[�����P(gu��n)���w�S��(x��)���ɷքe�ṩ������Ȱ�������̼Դ����֧���[����(x��)���е�TCAѭ�h(hu��n)���x�����⣬��Ƥ���ѳ�����(x��)���܇���֬����(x��)�����[���l(f��)չ�ṩ֬���ᡣ�෴������(x��)��ͨ�^���N�C(j��)���ӱ�CTL�錧(d��o)�Ě���������ጷŴ��x�a(ch��n)����Ȯ��������ᣬ�@Щ���x�a(ch��n)�������(qi��ng)�{(di��o)��(ji��)��T��(x��)������ϵ��(x��)����ه���������ƹ��ܡ�������Կ�ԭ�̼��������������w����PD1��Ҳ����(d��o)��TME��T��(x��)���Ĵ��x�p����Ŀǰ���҂�߀������ȫ����TME��(n��i)��ͬ��(x��)��֮�g���x��?d��ng)_��Ŀǰ�о��w��(n��i)�[�����x��һ�������ǟo���_���z�y���Ĵ��x�ǁ�����(x��)��߀��TME��(n��i)��������(x��)������ˣ����z�y���g(sh��)���u���@�N���x���|(zh��)�ԡ�
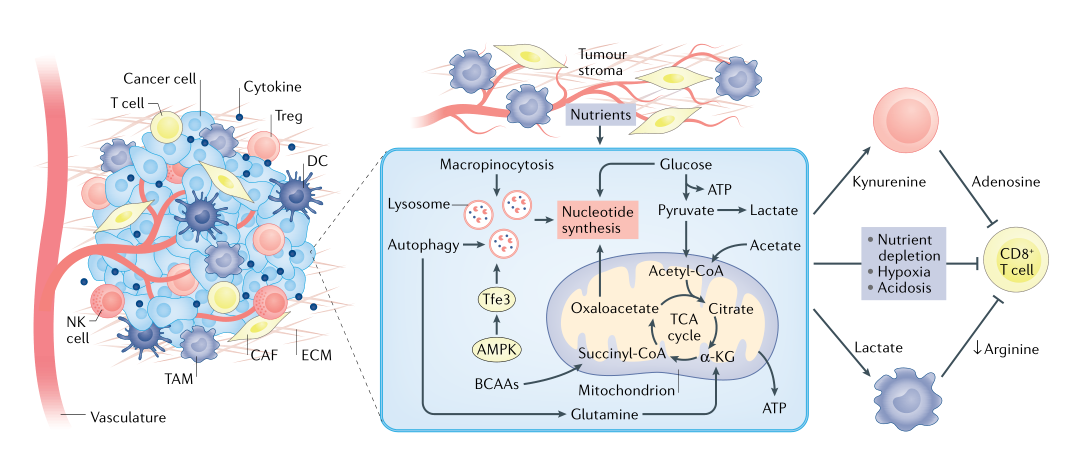
�D4 TME��(n��i)��(x��)���Ĵ��x��?d��ng)_
�D(zhu��n)�ƵĴ��x�{(di��o)��
���^ȥ�Ď�����[�����x�о���һ�����d�I(l��ng)�����D(zhu��n)���о����@�ǰ��Y����������һ����Ҫ���ء��D(zhu��n)����һ����ԭ�l(f��)�[����(x��)���U(ku��)ɢ���^�l(f��)��λ�ĵ�Ч�^�̣����x���ƬF(xi��n)�ڱ��J(r��n)�����[����(x��)���D(zhu��n)�Ɲ��ܵ��ϵK�����x׃���c�D(zhu��n)���^���е�ÿһ���B�m(x��)�Ķಽ�E�^�����P(gu��n)(li��n)������Ĥ�����u�ͼ�(x��)���w�Ƶ��܇���Ѫ�ܻ��ܰ�ϵ�y(t��ng)�����w��(n��i)����������ѭ�h(hu��n)�����棻Ѫ����B���^�l(f��)���[����λ�Ķ�ֲ��
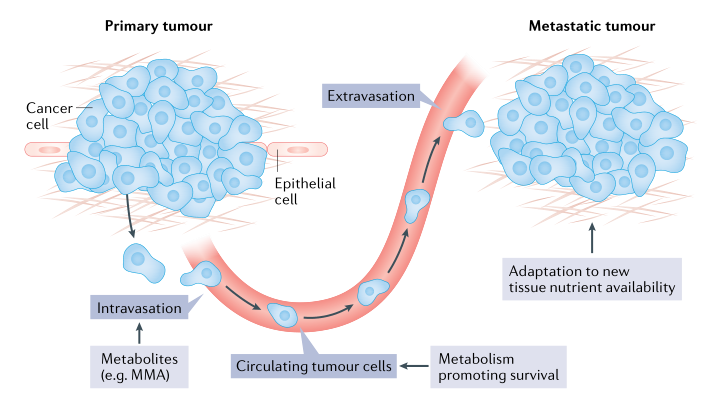
�D5�[���D(zhu��n)�ƵĶಽ�E���x�{(di��o)��(ji��)
������x��
���_ʼ�����xø���[���Y�ί��������������ί����c(di��n)�������ڶ�Nԭ��ᘌ����x�����ˎ���١�����������ǵ�һ�����ڰ��Y�ί���ˎ�Ȼ���M(j��n)һ���о��l(f��)�F(xi��n)���������HӰ��[����(x��)����ҲӰ���������ֳ��(x��)����ͬ�ӣ����ڌ������M���Ķ��ԣ������������x�����xø���ί�Ҳ�ܵ������ơ�
���棬ͨ�^�����ʳ�еĽz��������Լ���ͪ���{(di��o)��(ji��)�[���M(j��n)չ���о��ָ��F(xi��n)���������磬�����ٰ����ӌm��(n��i)Ĥ�������װ������ٰ��Լ�������ϵ��Ѫ����С��ģ���У��ȍu�ؿ���Ч����PI3K��̖ͨ·����ͪ�ʳ��SGLT2���Ƅ������PI3K���Ƅ��į�Ч���@�ɷN���Ƅ����ɽ����ȍu��ˮƽ�����⣬�����cijЩ���Y�İl(f��)����֮�g����(li��n)ϵ����С��ģ���У��o���֬�ʳ������ԭ�l(f��)���[�������L���D(zhu��n)�ơ�����MUFA���ʳ���ܛ]����̎����?y��n)����������܉��ֹ�F�������Ķ����ڵ������[�����L���D(zhu��n)���L(f��ng)�U��
�����p��ͨ�^���ƾ����w��(f��)����I���{(di��o)��(ji��)�[�����߱������[���A(y��)�����ί��������p���ί���ɽ��ͼ�(x��)����(n��i)�춬����ˮƽ������ͨ�^�����춬����ø���ɜp�ٰ����춬����ˮƽ���Ķ��ӏ�(qi��ng)ˎ����С���[��ģ���еį�Ч����Ȥ���ǣ�һ�(xi��ng)�о��������ٰ���(x��)����(n��i)�춬�����Ŀ����ԛQ�����[�����D(zhu��n)�Ɲ������҂��Ɯy���ЙC(j��)��x���D(zhu��n)�\(y��n)���ף�OCTs���߱��_(d��)�����Ƕ����p�Һ��춬����ø���[���ί���Ч��ǰ�ᡣ���ā��f���@Щ�о�������������x�ί���Ҫ�����Ի��t(y��)�������������x���_���[����(x��)���͙C(j��)�w���xĿ��(bi��o)�����Y(ji��)���z���C(j��)�ƺ��o(h��)���(bi��o)��(zh��n)�ί����D6����
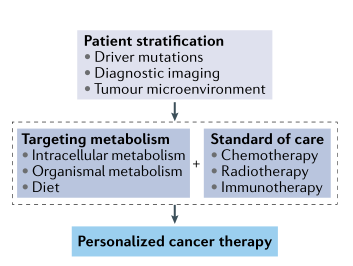
�D6ᘌ��[�����x�Ă��Ի��t(y��)������
���Y(ji��)
�[�����x�ѽ�(j��ng)��WarburgЧ��(y��ng)�ĺ���ģ�Ͱl(f��)չ��Ŀǰ���[�����x�ľ��(f��)�s�Ե��о���δ��߀�������P(gu��n)�I���}��Ҫ��Q���F(xi��n)���ѽ�(j��ng)�J(r��n)�R��TMEʩ�ӵĴ��x���ƺ�TME��(n��i)��ͬ�ļ�(x��)���M�����Ӱ��[���M(j��n)չ����(y��ng)�����P(gu��n)���g(sh��)��ʹ�˂��܉�l(f��)�F(xi��n)�µĴ��x���ף��l(f��)�F(xi��n)�[����(x��)�����[����ʼ���M(j��n)չ���D(zhu��n)���^������ʹ�õ���;�������xˮƽ׃����������ӻ����L(f��ng)�U�ģ��@���f��һ����δ��ȫ�������I(l��ng)����δ�������ܕ���l(f��)չ��һЩԴ���[�����x�о��ļ��g(sh��)���뷨���ѽ�(j��ng)�����d�I(l��ng)������ߴ��x���ɼ�(x��)�����x���ЙC(j��)�w���x�a(ch��n)����Ӱ푡��ڽ�����ʮ���С���Ӵ��x��@һ���S��F(xi��n)����������W(xu��)���z���W(xu��)����������T�x�֣����^�m(x��)������W(xu��)�Ͳ���W(xu��)�ęC(j��)���о��аl(f��)�]�e�O���á����������^ȥ�Ď�ʮ�����Щ��������ͼ����a(ch��n)����Ӱ푵�ˎ�������͡�ˎ������p�Һ������SGLT2���Ƅ�������ᘌ�С���Ӵ��x��ġ�



