�P���҂�
�īI����ح�c����Ⱥ�c���K����
�c�����{�����w����������C���е���Ҫ��������õ���ҕ���c�����K֮�g���p����Ҳ�����⡣���K�������c-���S�IJ�ͬ�P�I����Ӱ푡��c�������a����Ҫ��Դ����ʳ�ɷ֡�������x����ػ�������ԭ����֪��ͨ�^�T�o�}�\�͵����K�����K�M��푑�����đ֭��Ϳ��w����ˣ����ֽ������c���������ͨ�^�{���c�����ρ����M�c-���S�ķ��B���ܺ͜p�ٿ�ԭ���ӡ��෴�����K������Ҳ���{���c������M�ɡ��w��ƽ���Ɂy��ʹ�cǻ�ȿ�ԭ���_���K�����¸��K�����ܓp��������K�������c������B�Ժ�đ֭��Ĕ_���ѱ��C���c�N���K�������P���M�ܾ��_�ęC���ںܴ�̶�����δ��Q���l����Life Sciences���@ƪ�C������ӑՓ�˽������c-���S�Ĺ���ָ�y��ͬ�r���]�ęC����������K�����IJ����������c��ʧ�{�ڸ��K��ͬ��׃��B�е����á����⣬߀ӑՓ���A�����K�������س̶ȵ����ί�������
�������_���_������WRavinder Nagpal�F���2023��5����Life Sciences�ڿ��ϰl���}�顰Gut microbiome as a therapeutic target for liver diseases�������£�����Ҋ�β��c�c����Ⱥ�ęC���M����̽����ԭ��朽ӣ�https://doi.org/10.1016/j.lfs.2023.121685��

01 ǰ��
�c�����Ա��J���dz����X֮���҂����w�ĵڶ����{�؆�Ԫ������c���Ȱl���Ļ�ӿ���Ӱ��҂������������@Щ��Ӷ������c�������ӵģ�����c����Ⱥ�������Q�����w�ġ��ڶ����X�������o�������M�е��о��������c������M������ꐴ��x��ʳ����̖���c��Ƥ���ϵĹ��ܵ������ԣ��Լ��f�{��������ϵ�y�Ĺ��ܡ��c������ͬ�r�y��������к����������K�������ı����Q�����˵����w������r�����C�������c�����Bʧ�{ͨ�^�����c-���S���c-�X�S���c-Ѫ���S���c-���S�c���Nθ�c���Լ���θ�c����Ⱦ���P��
�c���S���L���c��֮�g���p���������T�o�}�S�֣����S�\ݔ�cԴ����̖���ӂ��f�o���K��ͨ�^���w��đ֭���ڵ�ʮ��ָ�cС�c�����M�и��K�������c����Ⱥ���Ĥ���c��Ƥ��������x���ԭ�\ݔ���ʳ�ɷ֡�����ϵ�y��B�������������{���c���S�Ĺ��ܵĎׂ��P�I���ء��cǻ�y�����������ԭ��δ������δ����ʳ��ɷ֣����x�K�a���Լ����c��Ƥ��Ó�����Ƥ�������cճĤ���c��Ƥ��Ѫ�܃�Ƥ�ӹ�ͬ�γ�һ���ӑB�����x���Ե�����ϵ�y��ֹ�c������Ⱥ�Ϳ�ԭ�M��ѪҺ��Ȼ�����c����Ⱥ�M���Ɂy�����Bʧ�{��������һЩ���ؿ��ܕ�ʹ�@�N�Y�����c�����ϐ��������²��������c���ļ������³��F���C���������c���B©���ߝB�ԣ�ʹ��ԭ������������Ĵ��x�ﵽ���K��K���¸��K�װY�ͼ������mȻ�c�����������Ըβ��е��������ў�����֪�������c-���S�ڸ��K���е����ÙC�ƺ���Ҫ�Ե��J�R�в����_��
02 �w��ƽ��h���µ��c-���S
�҂����T�o�}����һ�����������S�c�����K֮�g�M���p����̖���f��ճĤ���c����Ƥ�Ȍӡ���ճĤ����ϵ�y�̓�ƤѪ�܃�Ĥ�Ǹ��x��ǻ���Ё��Ը��K���ж���ԭ��������P�I�ɷ֣�ֻ���S�x���Է����M���c��ѭ�h���c-���S�ĽM����D1��ʾ��
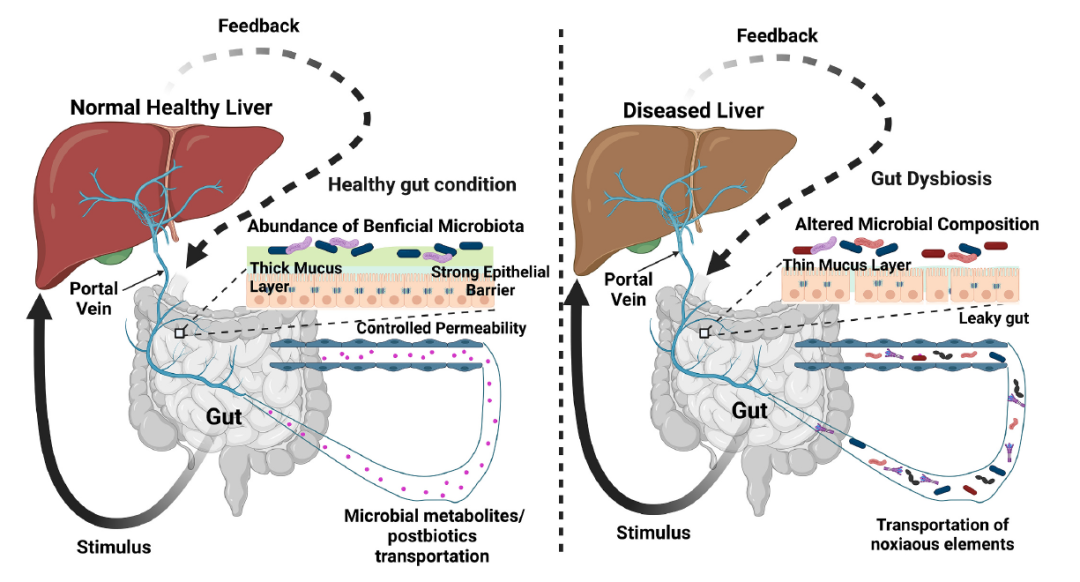
�D1. �c-���S��ͬ���ɲ��ֵ�����ÈDʾ��
���S�����Ͳ������װY�����ľ�Ⱥ�����ăɴ�ԭ�t�У���i�����Ƽ����c��Ƥ����������ã���ii������ϵ�y����Ч�ԡ��������������������x�ǻ���ճҺ�����M���cǻ��������������ֵĵ�һ���������c��θ���������_���нM���ăɌ�ճĤ�ӡ���С�c��ճĤ���Dz��B�m�ġ���С�c�У�ճҺ����С�c�ײ������[�C��픲����ڣ�Ȼ���ڽqë֮�g�����Ƅӡ���ˣ��që�ļ�˲������DZ�ճҺ���w��
2.1ճҺ
ճҺ����������c��Ƥ������������ڣ���һ�N���Ҏ��߶�ؓ늺ɵ��ǵ��ף����Q��ճ���ס������ͺ�Ĥ���P��ճ����ͨ���ԽM���ͼ����خ��Եķ�ʽ���_�����b����20�N��ͬ��͵�ճ�����У�MUC-2����Ҫ�����c���M����Ƥ�����Һ�ӷ����Һ���ǵ��ס�ճ���Įa�������P��Ҫ�ģ�����@ʾMUC-2ȱ��С��Y�c�İl�����ʺͻ��װY�ԽYֱ�c�����L�U���ӡ�
�c�o���ă��Һ�Ӳ�ͬ�����Һ�ӱ�����������ֳ��Muc2�������װ���ĵ����ѽ�IJ��ִ��M�˔U���������S���ﴩ���|�ӡ�һ�����������M��ճҺ���z����������ճ��������ȥ�����ǣ��Ķ����r�S����ճҺ�ӵĺ�ȡ����⣬ճ���׆��DZ��ض��Ĺ�����������������Դ���Ķ�����һЩ�������ڮa��ճ���ס��������ľ��ǽ�������Ҳ�����ڏIJ����������w�S�Ы@ȡ�~������������⣬��K�aƷ �����֬���SCFAs�����Ժ����ؔUɢͨ�^ճҺ�ӣ����Y�c�c��������������Դ��SCFAs�錧�ĽY�c�c�����ϱ��_��G����ż���w�ļ��� ��GPR41��GPR43���������� ���x�a����Ԟ鼚���������ṩһ���o�ܵ���ϡ�ճҺ�ĄӑB׃����ճ���ij��m�a���ͽ�����S�֣��@ʹ�������Ó���ճҺһ��������Һ����C�ƣ��絰��ø����(�~�G�نΰ�������ɫ��������ܽM���Ȱ��װ�)�������I߀ԭ(���T�ݗU��)�����ջ���(��Ͽڷ����c������Ⱥ��)���@�������ṩ�˃������벢���Һ�Ӵ�
2.2���������ɷ�
�Һ�к��б�������ڵĶ�N������ӣ��Լ����cճĤ�еĝ{�����a���ķ�����������A��SIgA�����@Щ���������ڷ������ϵĹ��������ԡ�SIgA ���������ų�ܣ���ͨ�^һϵ���l�����¼�������������ճҺ������ ��/��ͨ�^��������ֹ��ԭ�w�Ͷ����M���c��Ƥ���������⣬�ض�����Ȼĸ��ι�B�@�õ�SIgA�x���Ե��c��������ã������M�������o���c�����D�� ��߶�ֳ�ĭh��������������Ⱥ���^���̼��c�����P�ܰͽM���a��IgA����ˣ��Һ����һ����ܵĭh����������ṩ���ض������B������������֮�g�V��������ƽ�_��
2.3С�c��Ƥ����
�Һ���µĆΌ��c��Ƥ�����ṩ����һ��������������ϣ���ֹ�M���cǻ�к���ԭ�M���T�o�}���@���c��Ƥ�����нqë���[�C�M�ɣ�����λ���[�C�������c��Ƥ�����Ըɼ���������¡��mȻ������c��Ƥ�����������Լ������������������ό��ӽM���c�cǻ��������_���@���������ϵ�������ه�ڼ���-�����B�ӏͺ����е����|�ąf�{�О飬�����p϶�B�ӡ�𤸽�B�ӡ��o���B�Ӻͼ������������[�C-�që�S��Ƥ�����gɢ�����nj��T���c��Ƥ������IEC���Vϵ����Ҫ�Ƿ�����IEC��������������ϼ������c�ȷ��ڼ����������������c������ϵ�y�ĽY����λ�����Q�顰�c��Ƥ���Ϲ��ܡ����c�ȷ��ڼ��������{���ȷ���ϵ�y�ļ��أ�������������ϼ������ڵ�𤵰�ס������ﵰ������������������������c��Ƥ����͵�������������á��@һ���Ϲ����ܓp����Ҫ�����c©����r�»�ͨ�^һЩ����������ֿ��܌��¿�ԭ���������λ�M���ӵ��Ĥ�ӡ�
2.4����ϵ�y������Ⱥ�Ŀ���
������������Ƥ�Ⱥ��ЌӼ��������ڼӏ��c�����ϡ���Ƥ���ܰͼ������c��Ƥ����ጷŵĴ̼��Լ��������������������cNK�������w�������w����á���Ƥ�Ȇκ����ɼ�����ͻ��ֱ�ӌ���ԭ���ӏĹ�ǻ�кY�x���D�Ƶ���ͻ�������ˣ��������ܰͼ����͆κ˼���������һ�����ʳ������ԭ��ǰ����ʿ��Ȼ������һ�l���o����������ϵ�y���Ќ��еļ����ṩ�ġ��ܰͼ���(��Ҫ��CD4+ T����������Th17������Treg����)����ԭ�خ��Բ�׃��NKT�������Ĥ���P�㶨T����(�R�eMR1�ʬF�ĺ��S�ش��x�a��)�ǹ��Ќ��е��P�I�Ǽ�������Th17���ڵİ������������o���B�ӵ��ʹ̼��c��Ƥ�����������c����Ƥ�c�ֹ��z���������ÿ��T��Th17�������MIgA�;ۺ����������w(pIgR)���cǻ�ȵķ��ڡ���T-reg����������Դ�Լ����R�e������ԭ��������������������T�����������ܼ����R�e���ṩ��ǻ�ȷ�������ԭ�������ԡ��c�����ܰͼ�������Ⱦ�ķ���Ҳ�ܿ죬��������������T�����Ĵ̼��a���������ӡ��c������Ⱥ�Ɂy���e����������Խ��ͣ��c�U���ơ���׃�ξ��T����ھ��T���M�U��������������ѿ�ߗU������θ����Ƶ��S�Ȝp���c�װY���c����IBD���IJ�����r���P���о�����С�c��Ƥ�����ϵ�Toll�����w(TLRs)��NOD�����w(NLRs)���Ը�֪����M��������ԭ�ʹ��x��׃��(�������P����ģʽ��MAMPs)�������Bʧ�{���g���܌���IBD����׃��MAMPs�����w��������|�l�˶�N;�������c�����ϱ��Ɖģ�ճҺ׃�����c�����������ڜp�١��c�����Bʧ�{Ҳ��ͨ�^���{Th17, Th1��Th2�ͼ��������{Treg����������IgA�����Mһ����������ˣ��c�����ϰ����f�{������(ճҺ����Ƥ����)������(IgA��������)�����߳ɷ�(��Ƥ�ȌӺ����w������)���ܣ����е��κ�׃�������������Bʧ�{��
2.5 đ֭��������{��
đ֭��(BAs)����ǰ���J����ͨ�^�z���γ���֬����֬���ԾS���ص��黯�����������ã��F�ڱ��J���Ǵ��x���τ������c-���S�Ĺ��������P�I���á�BAsͨ����Դ�ڸμ����е�đ�̴������Ըʰ����ţ�����ż�}����ʽ���ڵ�đ֭�С��a��đ֭��ĽM�ɺͶ���ȡ�Q�ڏ��c�������K�����ӷ�����·���Q���c��ѭ�h��95%��BA��С�cˢ��߅�类�����գ���ͨ�^�T�o�}ѭ�h�\�ظ��Kѭ�h��ʣ�µ�5%���_�Y�c���@�������BAs֮�g��������c�������ﱻ������x����ˮ�Ĵμ�BAs�����о��������Sđ֭���ȡ��c������M�ɺ��K�����������P��BA���Ķ��ٺͽM�ɿ����{�����w�c������M�ɡ�Ҳ���о��������c����Ⱥ�Ĵ��x���ԛQ����BA�ĽM�ɣ������������ȥ�Y�Ϻ�7��-ȥ�u��������BA�����������о�������c���y������ȣ��o��С���đ֭����@���������@���������ں����w���ᴼX���w(FXR)���Ƶ�픶��c��ه��đ֭���D�\�w(ASBT)�����{�����⣬�@Щ�о�߀�^�쵽���ڟo��С���У��c���yС�����ƣ�����Ⱥ�֏ͺ�BA�ؽ��ͣ�����С�����Ҫđ�}ţ����-��-��đ������һ�N��Ч��FXR���������Mđ֭��ϳɡ����о������������ظ��A����ʳ�ɷֿ����{��FXR���ӄ��������ı��������Ҳ����Ӱ�BA�صĴ�С���M��Ӱ푺�ھ��T:�M�U���T�ı��������߀���������ʳ���Ԍ�BA�؏ĸʰ����D׃��ţ���������@����������c��������Bilophila �����L����֮���ʳ���A��/�������{�����������ӛQ����ͬ�c������ķNȺˮƽ���ڱ���Ƥ���������պ�BA��׃����FXR��TGR5���w��֪���M������BA�ȴ��x�^�̡��װY�������ȍu�ػ��Եķ�����̖��������
03 �c��ʧ�{�ڸ��K�������������е�����
������³��F���C�������c�����Bʧ�{���c©�ͼ�����r�Ǹ߶��P�ġ���ˣ��c��֮�g�Ľ�������Ҳ�����⡣�S����K����Ҳ�c�c������Ⱥ�Ɂy���c�����Ϲ����ϵK���P���Ķ������к���ԭ�������������x���M��ȫ��/�T�o�}ѭ�hϵ�y�����K�������Mչ�Mһ���ӄ����c�����Ϲ��ܺ�����M���B�Đ���������ӑՓ�˰����ƾ��Ը�(ALD)���Ǿƾ���֬���Ըβ�(NAFLD)��Ӳ���ڃȵĸ��K�����IJ�������W���Լ������c�c������Ⱥ���c-���S�c�����������Ե��Pϵ��
3.1 �ƾ����x�c�ƾ����P��֬���μ���
�μ���ռ���|����70%����Ҫͨ�^����ø������Ó��ø(ADH)�⻬���|�W���P����ɫ��P450 2E1 (CYP2E1)���c�Ҵ�/�ƾ����������x�����^������øʹ��H2O2���ƾ���������ȩ�е�����Ҳ�ѱ��_����ADH���Ҵ���������ȩ����ȩͨ�^�����wøȩÓ��ø�Ļ����Mһ�����x�����ᡣ�@�ɂ��^�̶����M��NADH�����ɣ��Ķ��_�y��NAD+/NADH(�����������ʶ��������������߀ԭ��ʽ)ƽ�⣬���´��x�D��߀ԭ�Ժϳ�(֬���ϳ�)�������¾ƾ����P��֬���μ�������øCYP2E1��һ�N�T��ø�����Ҵ��Ĵ��ٶ��^�������Y���H�����^�����@�Nøؓ؟���x�����Եİlչ�����ض������Ҫ���ߵľƾ����������_���ж�ˮƽ�����⣬���ˮa���^�ߵ���ȩ�⣬CYP2E1߀�a�����N���������ڸμ����Юa������������B��ͬ�r��ƽ��μ���������ø�Ļ��Ժ͝�ȡ����c�����|��֬�|�l�����η�����ROS�������Mһ���ӄ��ˑ��������⣬ͨ�^ADH��CYP2E1�����������Ҵ��a������ȩ�c֬�|�^������͵����|����ã��γ��w�e�^���ȩ�Ӻ����������ԭ�����á�
�о�����NAD+/NADH��׃���������Ǹ��K֬���ѷe����Ҫԭ�����C������֬�|�ϳ��܃ɷN�D����ӡ��̴�����Ԫ���Y�ϵ���- 1c (SREBP-1C)���������L����-1 (Egr-1)�{�صĻ�����_���ơ��Ҵ������|�l���|�W���P�ğo����SREBP-1C��λ���ߠ����w�������������v������D䛻��Ժ����ӣ������{֬�|����ı��_�����⣬Erg-1���{֬�����ɼ�������(��TNF- ��)��SREBP-1C�ı��_���о��ˆT߀�^�쵽��ƾ������M֬��������֬���ֽ⡣���a�������x֬���ᱻ�D�\�����K�������������������ɸ����������Ķ�ʹ���K��֬�������^�ء����˾ƾ������K֬�����ɵļ��������⣬�ƾ�߀��ע��䌦֬�|������ݔ���Ĝp�����á��ƾ��Ĵ��������ѱ��^�쵽�p��֬�������a����֬��(����)���@�����c�μ�����-�������½����P�����⣬�о������ͨ�^Ӱ�VLDL�ĺϳɺͷ��ځ�p�ٸ���������ݔ������C���в�������ƾ����x��ALD��������C�ƵĿ��Y��D2��ʾ��
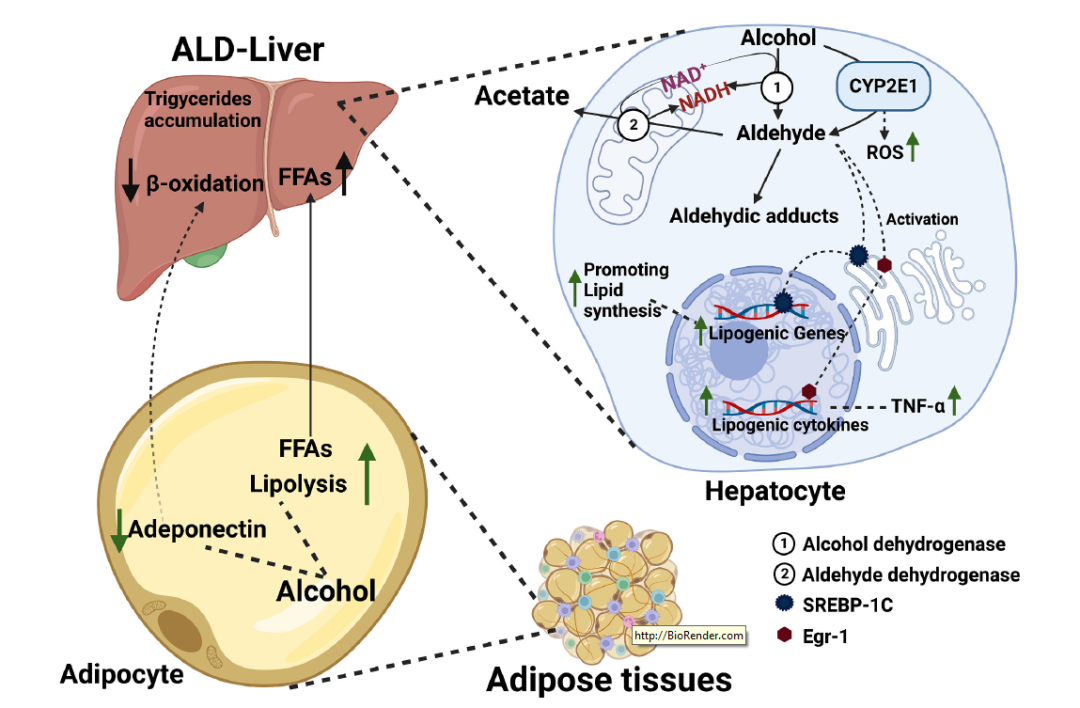
�D2. �ƾ����x�cALD�IJ���������
�ڸ��K�w�S���Č��H�Y����F֮ǰ��ƾ͕������c������Ⱥʧ�{�������M�о�����˴���ƵĻ���/�����c����������Եļ���׃����׃�ξ��T�����ă������ӣ���ھ��T�͔M�U���T�ı����p�١�һЩ�о����J����صľƾ��Ը����c�����c�����p��U�����������S���Լ�����U���Ĝp�����P�����⣬�����Ծƾ��E�õ��о����������ԭ�w����������c�����^�����L����ͨ�^�wѭ�h��λ���ھƾ����P�Ըβ������У�©�c��r���c��ͨ�Ԯ��������ǹ��J�Ġ�r����֪�ƾ���������Ȼ�������ף���Reg3a���Ķ��������Bʧ�{�����������c�c��Ƥ����������ã��Ķ��Mһ���T���c���װY���c���װY���κ˼����;��ɼ����ڹ��ЌӾۼ����a��TNF-�����������Ϲ����ܓp���c��ͨ�����ӡ��@�N©�c�����ڿ�ԭ�����x����������λ�M���T�o�}ѭ�h�����_���K���ƾ�������c�����Bʧ�{Ҳ��׃��đ֭�᷀�B��ʹ���K��¶���ж���đ֭���С�đ֭��ȥ�Y��߀���_�y�c�����е�FXR����;�����Ķ�����Ѫ�{��FGF-15��ˮƽ���Ķ����Ӹμ�����Cyp7a1�Ļ��ԡ�
ͨ����r�£��o����ԭͨ�^�T�o�}ѭ�h���_���K���������@Щ��ԭ�����ո�����(KCs�����v���ɼ���)�Y�x����֪�@ЩKCs���������ԣ��������������ÿ�N��ԭ���з����������h���IJ�ͬ���@ЩKCs���Գ������ױ���(M1)���ױ���(M2)���^���ƾ����^�l�ԓp��(��ȶ��ء��I�B���ӡ���������Ⱦ)�Ĵ��ڿ��|�lKCs�����M1���ͣ�ጷż������ӡ��������غ�څ�����ӣ���ѭ�h���������ɼ��������⣬KCs�����a��ROS���Mһ���ӄ��μ������������������ɵ�ROS��ʹ���c�� -������ø(�����oøaÓ��ø���ⶾ�A�ؙ����D��ø-1)�^����������֬������e���Ķ����¸�֬��׃�ԡ�
3.2�Ǿƾ���֬����
NAFLD���Mչ�A�ΰ���֬���e��(֬��׃��)���Ǿƾ���֬���Ը���(NASH)�ĸ���Ӳ����NAFLDͨ�����J���Ǵ��x�C�����ĸ��K���ͣ�������c���x��������֡�2������Ѫ֬�������й�ͬ�ęC�ơ������ֹ��NAFLD�Ĵ_�ЙC���Բ������Ȼ����NAFLD�cALD��һЩ��ͬ�IJ�������C�ơ��D3���Y��NAFLD�Ŀ��ܙC�Ƽ����c�c����Ⱥʧ�{���Pϵ���о�߀����˶���ײ�����f������ԓ��Փ�����K(��һ��ײ��)�е�֬���e�ی���������׃����Ӱ푸��K�ȍu������������¶�ڵڶ���ײ���r�Mչ��NASH���ڶ��N�����DZ�¶�ڃȶ��ء�څ�����ӡ��������ӻ��κ������к����ӡ��о������c�����Bʧ�{���H�cNAFLD�İlչ���P�����Ҿ��в���W���á���NAFLD���ߵ��c������M�M���У�����M�����ԵĜp���ѽ����ձ�ע�����ͬ���о����^��NAFLD��������֮�g��ͬ�����T���V���ƻ�ٵ�׃���ԡ���ͬ�Ĉ���J����θ�����(Ruminococcaceae)�Ĝp�١�׃�ξ��T(Proteobacteria)������T(Fusobacteria)�ĸ����cNAFLD�İl�����P���M���^�쵽��������Ԝp�٣���һЩ������M�U���T���S�Ⱥͺ�ھ��T�Ĝp���cNAFLD�İlչϵ������Ȼ�������ÔM�U���T:��ھ��T������������NAFLD����������������־���Դ��ڠ��h��
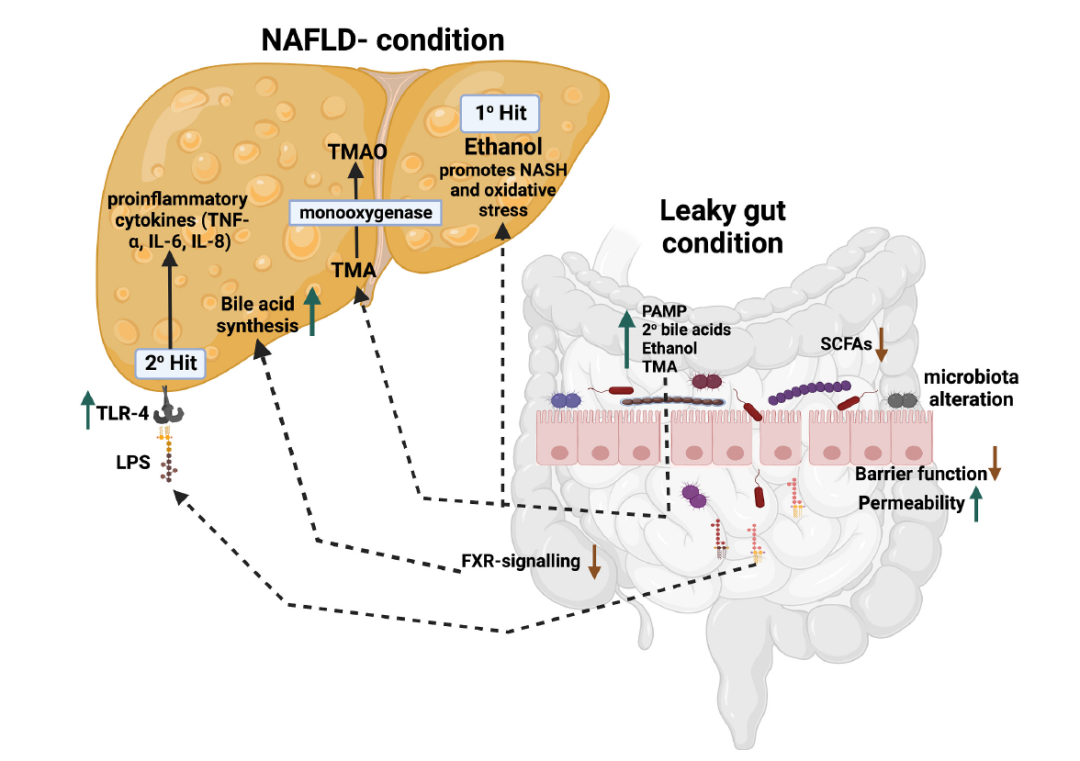
�D3. NAFLD�lչ�ęC�ơ�
���֣��e�Ƿ���������c�����Bʧ�{���ѱ��J����NAFLD�lչ����Ҫ���ء�Ȼ������ͬ�w��ָ���ķ��ֻ��ߵ����Bʧ�{ģʽ������ͬ�����⣬�c������Ⱥʧ�{Ҳ�U���˷Ƿ��ֻ���NAFLD�İlչ���cNAFLD���S������Ⱥ��ֲ�����ί������������ί����w���P��������Ⱥ�S����ֲ���P���о��C�����c�����Bʧ�{���ǿ�������NAFLD�lչ��ԭ��
���]�����Bʧ�{����Ҫ�ԣ��J���N���ʽ����(��֬������w�S�ʳ���w����ӡ�������Ƶ�)���܌������Bʧ�{�����MNAFLD�İlչ�Ǻ����ġ������ʳ(��֬������w�S�ʳ)�Ĕz�롢��Ҏ�ɵ��ʳģʽ����˯�����ʽ�Ϳ����ص�ʹ���nj��´��x�C����(���֡�����)�l���Ħ�-�����Խ��ͺ��c�����Bʧ�{���P�I���ء��ʳ����ֱ���{���c���Ę�־������Ⱥģʽ�����xģʽ�ʹ��x��أ���K�����c��Ѫ�����Ϲ��ܣ�ʹ���x����ء�څ�����ӻ�����ͨ�^�T�o�}ѭ�h�D�\�����K���о��������ڸ�֬�ʳι�B��С��ģ���У����Bʧ�{���P���c��Ѫ�������Ɂy������LPS���գ����Ѫ����LPS�Y�ϵ���ˮƽ�����{�μ�����TLR-4��TNF- ���ı��_���Ķ����l���K�װY��ͬ�ӣ���NASH������Ҳ�^�쵽��Ҏ�t���c�����ϡ�©�c�w����Ѫ�{LPSˮƽ���ߺ�TLR-4�ĸ߱��_��һЩ�о�����Oscillospira�NȺ�����½��cDorea�����Լ��M�U���T:��ھ��T�����p���cNAFLD��NASH���P�����⣬һЩ�о��ˆTԇ�D�����Bʧ�{ģʽ�c�Mչϵ����������ӋNAFLD��NASH�ć��س̶ȡ�Ȼ�����@Щ���P�о���Ҫ�м��Ĕ�����ጣ��������ģʽҲ��ه�������ı�����
���x;���ĸ�׃�����Ҵ����ɵ����������֬�������ɵĽ��͡�đ�A���x��đ֭�᷀�B���ɁyҲ���J���cNAFL�İl�����P����������ڻ���NASH�ķ��փ�ͯ�У������Ɂy�c���а�ϣ�Ͼ����^�����L��ѪҺ���Ҵ�������ߡ������յă�Դ���Ҵ�ͨ�^�T�o�}�D�\�����K���ӄ���������������̈́����о��C����SCFAsˮƽ�½��c���x�C������NAFLD�İlչ���P���@�NSCFAs�Ľ����cNAFLD��ԇ����������ʳ�w�S����������׃�ξ�Ⱥ�Ĵ������L�͔M�U��Ⱥ�Ĝp�����P���F���C��������SCFAs��NAFLD�����A�����ã��������}�oˎ�ɻ֏�֬��׃�ԣ����Ƹξ����w���Ժ����w�ι��ܡ��о�������SCFAs(�����})���{���K�Ǯ���ø�ı��_�����⣬SCFAsͨ�^����GPR43����֬���M���е��ȍu����̖���Ķ��p��֬�������е�֬���e�ۡ�SCFAs(�����})������������p�p�c���װY���{����С������}ͨ�^�ӏ��c�����Ϲ��ܣ���ֹ���ػ�ԭ���^�c���������ρ��S���c���ȷ��B�����C��������SCFAs�Ĝp��Ҳ�Ǹ��K֬���e�ۺ��c�������Ɂy��ԭ�Ķ��T��NAFLD�İlչ���о��������x���g�w���e���������}����NASH/���w�S�����Mչ�о�����Ҫ���{�����á������������֬�����Ժ������������¾����w�����ܓp�����¸μ�����TCAѭ�h���g�w(������)���ڵ���������g���������}���B�m�e���|�lHSC�еĿ�Ĥ��̖����(GPR91)����Ķ��T���װY����NASH/���w�S������Nˎ��(���J������̴�Ρ�̴�㴼��Scoparone��)����������GPR91��̖ͨ·�ί�NASH���о��ѽ�������@���ί����K�����������µĿ����ԡ�
đ�A�����w������ĠI�B���|�����K�a���dz�������đ�A����ˣ���Ҫ�����ɸ���đ�A����ʳ��Դ��M�㡣��֪���ķN��ͬ�Ĵ��x;�����Ԍ�đ�A�D��������đ�A����ˉA����֬�����װ�(TMA)��đ�A�z�벻������đ�A�D����TMA���µ��������öȽ������c�N�������P�IJ�ͬ���ء��F���īI��������đ�A�z�������Ɖ��c��Ѫ�����Ϲ��ܣ�ʹ��ԭ�����غͲ�ԭ�w���������K�����l���K֬��׃�Ժ��װY�����⣬��֬���ʳ�T�����c�����Bʧ�{���º�ھ��T��׃�ξ��Tռ������λ�������܉�a��đ�A-TMA�ѽ�ø�����ʳ�е�đ�A�D����TMA�������յ�TMA���_���K�����������Mһ�������Kø���μ���ø���x�����װ�-N-������(TMAO)��Ѫ���������װ�ˮƽ�ѱ������_��������r��ͬ���ٹ��ܵĘ�־��TMAOˮƽ�����c��Ѫ�ܼ����������I�K�������P�����S���о��ˆT�J��TMAOˮƽ�����cNASH�İlչ���P����ǰ��������֪���Bʧ�{��Ӱ�đ֭�᷀�B��BA�أ���鲻ͬ��������x��ӕ����Ӵμ�BAs�ĝ�Ȳ��p��FXR-FGF19��̖���о�������BA�V�Ɂy��BA��̖ͨ·�ܓp�����cNAFLD�����Bʧ�{�Ͱlչ���P��Ȼ����BA�V�cNAFLD��B֮�g�����P��������δ��ȫ�U����
3.3��Ӳ��
�oՓ�p���IJ���(ALD��NAFLD��NASH��������Ⱦ)��Σ���Ӳ�����ǸΓp������K�M����;�����μ���˥�ˡ��w�S���������Y���Mչ�Լ��ι����ܓp�Ǹ�Ӳ���ij�Ҋ�����������������@�İY��ι��ܣ���Ӳ��ͨ���֞������(�o�Y��)��ʧ������(�аY��)���c��ǰӑՓ�ĸ��K����һ�ӣ������c�����Ϲ��ܐ������c���B©������������x������K����λҲ�ڸ�Ӳ�������б�ע������⣬һЩ�������Ӳ���İlչ�cLPS�D�\�����K��TLR-4�錧����̖ͨ·���T��ϵ������TLR-4�ڸ��K���|�����ͷnj��|�����Ͼ��б��_������ԭ�w���P����ģʽ(PAMPs)��Σ�U���P����ģʽ(DAMPs)�з�����Ȼ�������Ǡ��(hepatic stellate cells, HSCs)ͨ���������g�P�g϶������Ӳ���İlչ�������P��Ҫ�����á�HSC TLRs�����w�cLPS��������|�l��̖�����������������(IL-6��IL-8��TNF-��)��څ������(MCP-1��MIP-2��ICAM-1)�Ϳ���������(bcl-2)��ጷš��������Ѫ�ɼ���ጷŵ�څ�����Ӻͼ������������ڰ����Ľ����������Ɖĸμ�������ͨ�^�����oֹ����Ѫ�ɼ����Mһ���ӄ��w�S�����������⣬TLR-4����ͨ�^TLR4-MyD88-NF-kB��ه�C�����{TGF- ��1�����wBAMBI (Bone Morphogenetic Protein and Activin Membrane-Bound Inhibitor�����ΑB�l�����ͼ�����Ĥ�Y�����Ƅ�)���Ķ����MHSC��TGF-��1�̼����������l���C����D4��ʾ�������M�о���������-�����Խ��ͺͦ�-������׃��ͨ���c��Ӳ�����P���о��ˆT�^�쵽�c�U���ơ��c����ơ���������Ƶĸ�Ӳ��ģ��ռ������λ����Ruminococcaceae��Lachnospiraceae�ĸ�Ӳ��ģ�̈́t�p�١�
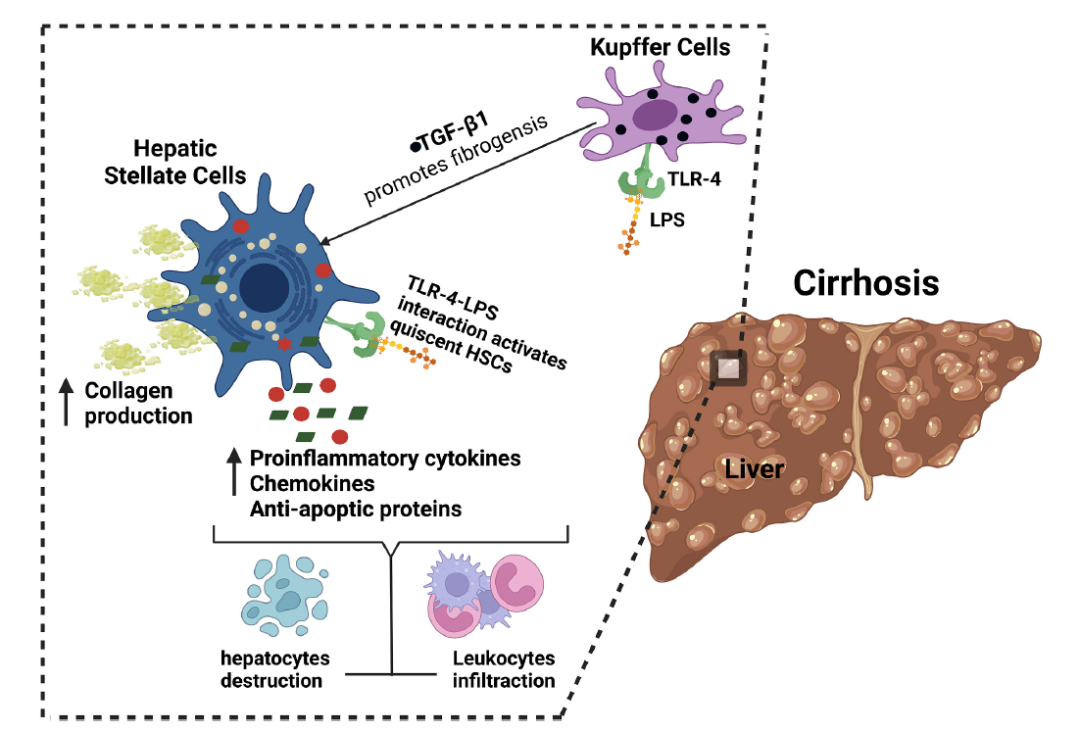
�D4. ��Ӳ���l���ęC�ơ�
04 �{���c-���S�IJ���
�����F�е�֪�R�����⣬��ǻ�������c������Ⱥ���c��Ƥ��Ĥ��Ѫ�����ϵȷ�������ö�����P�Ć�Ԫ����ͬ�������c-���S���нM���Y���������ڼ����l���rÿ����λ����׃��һ�ӣ����κΆ�λ�M����Ƶĸ��A�����Գɹ����A���������c���Ƹ��K�����ĸ��A��ʩ���P�Ī����о����Ը����Ƿ����c��������c������Ⱥ���c�����ϻ���c����λ��Ŀ���M�з���D5������ᘌ��c-���S�IJ�ͬ�ί����A��ʩ��
4.1.đ֭����̖
���K�����cđ�ش�С�U��ͽM�ɸ�׃���P�����⣬�������BAs�ѱ��_����ͨ�^����FXR��TGR5�錧��;�����{��̼ˮ�����֬�|���������x����̖���ӡ���ˣ�BAs��FXR��TGR5���ӄ��������ί�ˎ�������K�����K���P���x�Ɂy����NAFLD�����ͷ��ְY��đ֭�ٷe��һ�N������B������đ֭�����Д����¸�đ֭��e�۶�������K�װY��FDA���ʵ�UDCA (Ursodeoxycholic acid���ַQUrsodiol™)��һ�NFXR���ӄ������T��đ�}ݔ����(BSEP)����ˎ��ˎ����2/3 (MDR /3)�Ͷ�ˎ��ˎ���P����2 (MRP2)�քe��đ֭�ᡢ��֬��đ�A(PC)���ЙC��x��ጷŵ�đ֭�С�UDCA��ԭ�l��đ����đ����(PBC)�������@ʾ���e�O���ã�����ԭ�l��Ӳ����đ����(PSC)��������Ȼ�oЧ��Ȼ����norUDCA(ȥ��Ó��đ��)��PSC������Ҳ�@ʾ�����˹���ĽY�����������������đ֭��HCO3-�ķ��ڡ��Wؐđ��(OCA)��FDA���ʵ���һ�NFXR���ӄ����ѱ�̽�������ί�PSC���ߵ���ϣ����ˎ��о��ˆTע����ڽo��OCA��PBC���ߵĸι��ܵõ����ƣ�Ѫ��A������ø���������D��ø�ͦ�-�Ȱ����D��ø�Ļ��Խ��͡�III���о������@ʾ��OCA��NASH�����w�S�����ί�Ч�����á��c�ȷ���L�����ж���đ֭�ἤ��TGR5���McAMP�ϳɣ��̼��ȸ�Ѫ���ؘ���-1 (GLP-1)���Mһ�����M�����ȍu�ط��ڡ����⣬TGR5�����c���������P��������������c�����K��TNF����NF-��B�錧�Ĵ��������ӵ��T����đ֭�������TGR5���ӄ�INT-777 (6��-�һ�-23(S)-��-CA)�ڄ����п���Ч�������������p�ل��}����Ӳ����׃���������Y�c�ס��װY���c��(IBD)�̈́��}����Ӳ�������A�����á�
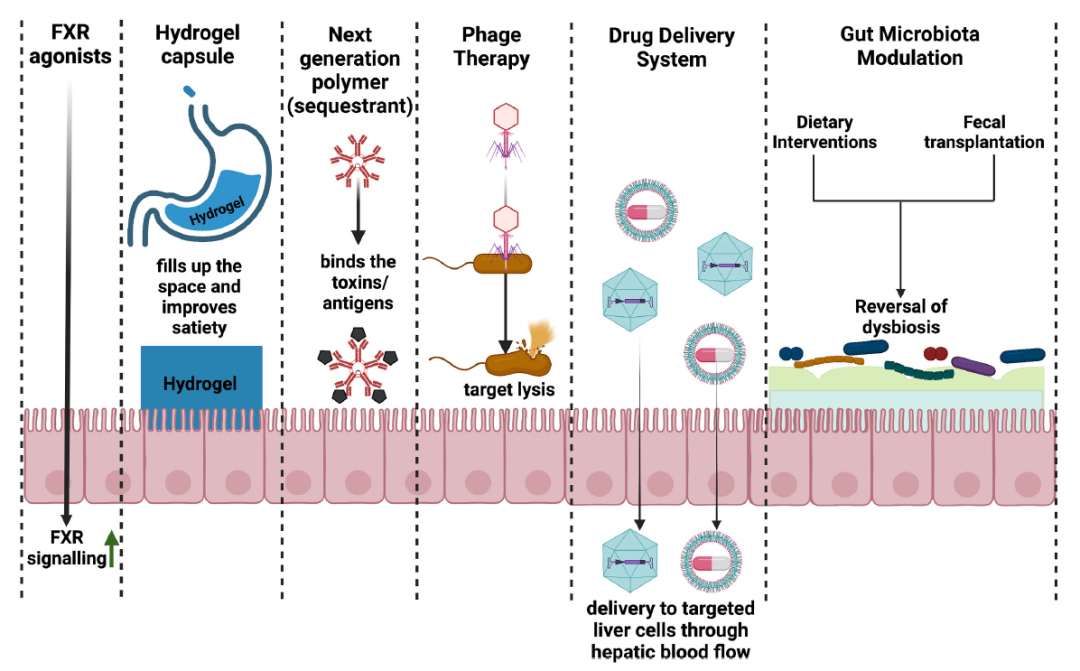
�D5. ᘌ��c-���S�IJ�ͬ�ί����A��ʩ��
4.2.�������τ�
�������ͷ��ֻ��ߣ�һ��������ǿ����ʳ�z�룬����ʳ�����S���w�أ�����Ѫ��ָ������ǰ�ڷ�ˮ���z�ѳɞ���ƴ��x�Ɂy�����ʳ�z���һ�N���ԡ��Ļ��W���v��ˮ���z��һ�N�ۺ�������ȼ��w�S��(�����w�S��)�c�����ύ���γ�һ�Nģ����Ȼ��ʳ�w�S��3D���|��һ���z�룬ˮ���z�z��Ѹ������ˮ�֣���Û����Mθ�w�e���ķ�֮һ���Ķ��ڲ����ӿ�·�����r�������С���Û���ˮ���z������Y���͙Cе���ܣ�ֱ�����_���c�����������������������Ķ�ʧȥ�˱���ˮ�ֵ�������ጷų�����ˮ���ڴ��c�б��������գ����w�S���|�t�S�S���ų��w�⡣���w��ԇ��У�ˮ���z��Ч�����ڳ�Ҋ���w�S�a�䄩����܇ǰ�ݡ��Ϡ��z���ϸ�¶���ǡ������ֻ��ߵ��R���о�������ˮ���z���ί����x�C������һ�N����ǰ�����ί���������Ŀǰ��ֹ��߀�]���о�����ˮ���z���������K�����į�Ч������Ч�����w�p�p���ȍu�������Եĸ��ƿ����cNAFLD�ĸ������P��߀����̽�������þۺ������τ��Y��Ŀ�ˌ��w���������@�N�ۺ���һ�����z�룬���Y��Ŀ�ˌ��w�����ҽY�ϵ��w�����S���ۺ����ڼS���б�ȥ�������磬đ���ġ�đ����đ����������đ֭��������������ã��@���������п��ܜp�p��ĸ�֬Ѫ�Y��đ�Yʯ���γɡ��о��ˆT�J�飬�@Щ�ۺ���Y��đ֭�ᣬ��K�c��ѭ�h���Ķ����Mđ֭��ϳɣ�����Ѫ��đ�̴�ˮƽ������ԇ�Ҳ�����đ֭�����τ��p�p�Γp����NASH�lչ�����ԵĹ�Ч��Colesevilam����͡�ˎ��ͽ���ˎ����2������ģ�����@ʾ���������á�FDA����WELCHOL (colesevam hydrochloride)������ʳ�o����ˎ���oՓ��Ƭ��߀�ǿڷ���҄����Ϊ���ˎ���c����ˎ������ˎ�����Ј���Q�ɽ���2��������Ѫ��LDLˮƽ������Ѫ��ָ����Ȼ������C���в���������ѽ�����ˎN���f����ͨ�^FXR��TGR5�錧����̖ͨ·�{����đ֭�����ˮ�Խ��͡��ۺ����Ԫ�c�Иˌ��w֮�g���x���������ʹ�ۺ����܉�ʹ�И�ʧ��Ķ���ֹ�����ܵ�����Ӱ푡�
��һ�N�ί��β��Ą��·��������ò������յ�̼�{���w�����@�N�{���w�����ԽY�����ﶾ�ز���K���K���������M���c��ѭ�h�����磬Yaq-001��һ�N�µĺϳɵIJ�������̼�����ȶ��ؾ��к����H�����������@������NASHС��ģ�͵ĸι����ޏ��ԸΓp�����Ј�����������^�l��đ֭�Ը�Ӳ����đ�ܽY�c�ׄ���ģ���У�Yaq-001�ɽ���Bacteroidetes:Firmicutes���������p��LPS�T����ROS�a�����@Щ�C���������@�N�ί����������p�p���K�������w����w��ԇ��C����Yaq-001�ڸ�Ӳ�������еİ�ȫ�Ժ������ԡ�Ȼ�����cYaq-001����Ч�ԡ���ȫ�Ժ����������P�����wԇ������M���С�
4.3ˎ�P���f��ϵ�y
ᘌ��c������ʧ�{(������)���װY(��Ƥ�|���ء�̴�������������̼����ӡ����[����������(TNF)����������(IL)-22��IL- 1R���Ƅ�)���w�S��(PPAR���ӄ����������ø���Ƅ����D�����L����-�����Ƅ�)����������(��ˉA��Sadenosylmethionine����Ȼ��������)�ͽ��(�������_�ᡢ�����������ȷ�)�IJ�ͬˎ���ѱ��yԇ�����ί����K������Ȼ�������ڲ�λ�خ����f��Ч�ʵ��¡����cˎ���ȷe�۲��㡢��ˎ�Ԯa����ˎ�������W���Լ��cÓ����������P�IJ���������ȫ���oˎ���ί��ɹ��ܵ����ơ����K����ˎ����x����Ҫ��λ���ЕrҲ���ܵ�ˎ����x����������Ӱ푣�����ˎ���ԸΓp��(DILI)��DILI�������z�����Ի����и��K�����ĽY�������⣬���ڸ��KѪ����׃�����_��׃�Լ������w��¶���ձ�ļ�����r�Mһ����K��ˎ���ڻ����w�ȵ�ˎ�������W�������@Щ���ƿ���ͨ�^�OӋ���и��Mˎ��ˎ�������W�İ���ˎ���f��ϵ�y���˷������^ȥ�Ď�ʮ�����ͬ���d�w����������֬�|��(�z����֬�|�w�������w)����֬�|��(�ۺ���/�մ�/���ټ{���w��)�����﹤��(��������)ˎ����fϵ�y�����x��Ľoˎϵ�y����܉�Խ�c�����ϣ��M��Ѫ���������cѪ�{���Y�Ϻ;W���Ƥϵ�y(RES)�������������ո����������ɣ����^�θ]�����ڰв�λ�e�ۺ�ጷ�����ȵ�ˎ���ʹˎ���c�����w����îa����Ҫ�����á�����ԓ�����R���D��������������·��棺a)�ڄ����о����^�쵽�ĽY�������wԇ��в����؏ͣ�b)�ضȡ��x�ӏ��ȡ�ѪҺ�е�������Ӻ�pH�����أ�c)δ�ܵ��_Ŀ�˸μ�����d)ˎ��Ĵ̼���ه��ጷţ�e)��ȫ���u��ӛ䛲��㡣
4.4.�c����Ⱥ�{��
�c����Ⱥ�ǛQ�����w���w���ܺͽ�����B���P�I���ء���־�Ե��c������M�M�ɿ����黼������r�Ę�־�����������w���ٸ�Ⱦ��Ӱ푡�ᘌ��c����Ⱥ�{���IJ����ڿ���θ�c���ͷ�θ�c����Ⱦ��������ϣ�����S������Ⱥ��ֲ(FMT)��������ڻ֏��c�D�y�����Ⱦ���P���c�����Bʧ�{������IBD�����x�C���������X��������Ҳ�@ʾ����ϣ���ĽY����һ����r�£��������ί���ڷ��z�ҽoˎ������ֲ�S������Ⱥ�������ؔ_�y�ˬF�е��к��ɷ֣�ʹ�������w�z�������Ⱥ��ֲ���֏ͽ����c����������ԡ��@�N�������@ʾ�ɸ��Ƹ�Ӳ�������X�����ߡ����C����������ιʳ�߹��Ǹ�֬���ʳ�Ĵ����M�мS����ֲ���K�������ȍu�������ԡ��T�o�}�߉����ͺȃ�Ƥ���ܸ��Ƶȷ���õ��֏͡��_�������ض�������B������������ɾ��w���������˙C�����ɾ��w���и߶ȵ������خ��ԣ��ɚ���Ŀ�˼�������Ӱ������Ⱥ�������ɾ��w�ɹ����Ʋ�Σ���ߵĶ�����ˎ�~�G�نΰ������U�����ӗU������̽���ɾ��w���ί�Ŀ�Ą����˿��ܡ�ͬ�ӣ�ʹ�ò������յĿ�����Ҳ�������{���c������Ⱥ�ĽM�ɡ����磬�����Ըβ�ģ����ʹ�����������{���c������M�M�����R��ԇ�ڶ����ġ��pä���S�C����ο�����յ�III���R��ԇ��У�����������������͡�ί�ʧ�����ڸ�Ӳ���@ʾ�����õ�Ч�����@Щ�����س��˾��п��������⣬߀���п��ͽ��̓ȶ��ص����á�Ȼ�����oՓ���ɾ��w����߀�Dz��������Կ����ض���δ�õ���ֵ��u�r��
���^ȥ�Ď�ʮ�������������һ�N������ӏ����F���������a���ڄ�������ģ���ж��@ʾ�����M���������ã��������c�����ϡ����ס�����֬Ѫ�Y���������ȡ���ˣ����������A���������Ʋ�ԭ�w���������Ϲ��ܡ����x��Y�϶��غ;S���c�����B�����������ԾS���c���S�Ĺ��ܡ�Ȼ�����c���������P��֪�R�����S�������Խ�Q�������}���@�������������r������׃�����@Щ�����w���������A��������־�Ҳ�����A�y�ί��ĽY�����@�N����Ĺ��������Q�鶨�x����һ��������(NGPs)���䌦������Ӱ���Ҫ�M��Ԕ�����b�����о����������о������ض��Ĺ�����Ⱥ�������Ĵ��M���ã��M�܌����K�������ض����������˽�dz����ޡ�ͨ�^���¼��g�����Ժ������M�л������������߯�Ч������ʡ����x��Įa�������ڱ����@ʾ��ԭ���������ߡ�Ȼ�������b�������x�����B�����g���ԡ��U��Ҏģ����ȫ�ͱO�ܷ�����ڸ��N���ƣ��@Щ����Ҫ���]��
05�YՓ��չ��
�c-���S���L���c��֮�g���p�������c����Դ����̖ͨ�^�T�o�}ݔ�͵����K�����Kͨ�^����đ֭��Ϳ��w��С�cʮ��ָ�c�팦���@Щ��̖���c-���S���О����c����M���c��Ƥ���ϡ�Ѫ�܃�Ƥ���K�Ȫ����P�I���c�ߵ�������{�����ɹ�ǻճҺ���c��Ƥ��Ѫ��ϵ�y��Ƥ���γɵĄӑB���x���Ե����ό��к��Ĺ�ǻ�������c�c��ѭ�h���x�_����ԓ�S���Ɖ��ѱ��l�F�c�ι����ϵK���K�������Mչ���P��ALD��NAFLD��Ӳ���Ďׂ�������������C������ͬ�ġ��³��F���C���������c������Ⱥ�Ɂy(���Bʧ�{)���c����ͨ�ԡ�đ֭��ش�С�ͽM���S���K�����Mչ�A�ε�׃�����˂�����̽��ᘌ��c-���S�IJ�ͬ�������A����֏��K����������ٿvđ֭����̖��ʹ���OӋ�ۺ�������c��������Լ�ͨ�^�S������Ⱥ��ֲ��������/��������/NGPs��׃�c������M���M�ܲ�ͬ�IJ���ȡ���˳ɾͣ�������һЩ�c�������P����Ҫ���}���@Щ���}�����������Č��H���á����磬BA�����������c���ص�Ƥ�w���W(���W�Y)���P���ѽ��_�����خ��Զ��ؽY�Ͼۺ�����٣������f�ͼ{���w��ϵ�y�����\��Ȼ�������
���⣬�ڄ����о��Ы@�õĽY�������wԇ����Dz����؏͵ġ����c���{�����Զ��ԣ��ɾ��w�ί��đ��������������Vխ����ԭ�����Դ�����߲����P���ܵ�һЩ���ơ�FMT������������A�IJ�������ϣ���ģ����ڵó��κνYՓ֮ǰ��Ҫ�M�а������wԇ��ڃȵďV���{�顣NGP��δ�����о�ĝ����������ڟo�����˹��l���·��x�����B�c������Լ����P�İ�ȫ�ԺͱO�܆��}������̎���_���A�Ρ����]�c������Ⱥ����Ҫ�Լ��䌦�c-���SӰ푵��۷e�C�������Ƅӌ������c������Ⱥ���A���\����ί������İlչ���dȤ���@Щ����������δ��������K�������A�������ƺ����ṩ�µ�;����



